1目的和范圍
1.1本文件規定了校準實驗室校準方法的管理要求,對校準方法的認可能力表述、現場評審和獲認可后變更等管理方式予以說明。
1.2本文適用于申請或已獲認可的校準實驗室(含醫學參考測量實驗室)、評審員和其他相關機構。
2校準方法的認可與變更方式
2.1認可能力范圍中校準方法通常應包含校準方法的名稱、代號(或文件編號),版本號(如發布年號、修訂標識等類似信息)不需填寫。認可申請書和評審報告中校準方法填寫示例:“鋼直尺檢定規程JJG 1-1999”只需填寫“鋼直尺檢定規程JJG 1”。
2.2當校準方法的版本號變更時(以下簡稱方法版本變更),在測量儀器名稱、校準參量、校準方法名稱和代號、測量范圍、擴展不確定度、限制范圍不變的前提下,實驗室在驗證具備新版方法規定的要求以及按新版方法實施校準的能力后,即可自行批準使用新版校準方法,不需要向CNAS秘書處提交變更申請。
2.3當方法版本變更導致認可能力范圍變更時,實驗室應按如下方式處理:
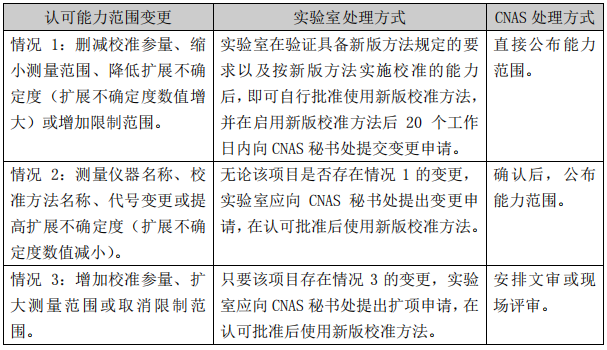
2.4當方法版本變更導致拆分或合并認可項目時,實驗室應根據認可能力范圍的變更情況,選擇本文第2.2 條款-2.3條款的方式處理。
3 對校準實驗室的補充要求
3.1實驗室應確保使用的校準方法現行有效(除非該版本不適宜或客戶有特殊要求),并且能夠滿足方法的要求。
3.2實驗室應對采用的校準方法建立控制清單,當方法版本變更時,應及時修訂該清單。清單修訂的歷史記錄應長期保存。當CNAS或其他相關方要求提供該清單時,實 驗室應隨時可以提供。清單中至少包括:
——校準方法的名稱、代號(或文件編號),版本號(如發布年號、修訂標識等類似信息);
——實驗室自行批準使用校準方法的日期;
——清單的修訂記錄(包括變更方法、增加方法、撤銷方法等):
3.3根據本文第2.2條款-2.4條款要求,實驗室應驗證是否滿足新方法的要求,還應分析方法版本變更是否影響認可能力,以確定是否需向CNAS秘書處提出變更或擴項申請。實驗室應保留相關的記錄。
3.4實驗室出具的校準證書中應明確依據的校準方法的版本號。
4 評審要求
4.1現場評審時,評審組應通過查閱方法控制清單以及方法版本變更的驗證記錄(監督或復評時)等方式核查實驗室對校準方法的管理是否滿足本文第2和3條款要求。通常可只查閱最近2年或上次評審以來的相關記錄。
4.2對于安排現場試驗的項目,《檢測/校準/鑒定實驗室現場試驗/演示試驗記錄表》中填寫的校準方法應包含版本號(如發布年號、修訂標識等類似信息)。
5 違規情況及處理措施
申請或已獲認可的校準實驗室出現下列情況時,CNAS 將根據問題的嚴重性要求實驗室限期整改或對部分/全部項目暫停或撤銷認可資格:
a. 未建立控制清單對所用校準方法進行有效控制的;
b. 使用前未對變更方法進行驗證的;
c. 經驗證不滿足變更方法的技術要求但仍使用的;
d. 未有效識別變更方法的技術差異,導致校準結果錯誤或不符合要求的;
e. 根據本文第2條款中相關要求,未經CNAS批準即開展校準活動的。
文章來源網絡,由中測校準平臺總結發布,供業內讀者參考交流,如有侵權,請聯系刪除